Módulo 9Ética
MÓDULO 9 – AULA 4
Pesquisa com seres humanos no Brasil
Quais são as instâncias nacionais que avaliam as questões éticas relativas à pesquisa com seres humanos e animais no Brasil?
Pesquisa com seres humanos – Sistema CEP/CONEP
A pesquisa com seres humanos é regida por legislações específicas e o órgão institucional associado de início de tramitação de projetos de pesquisa com seres humanos é o Comitê de ética em Pesquisa (CEP), que juntamente com o órgão centralizado, a Comissão Nacional de Ética em Pesquisa (CONEP), que está diretamente ligada ao Conselho Nacional de Saúde (CNS) formam o sistema CEP/CONEP. Esse sistema visa cumprir a sua principal atribuição que é a avaliação dos aspectos éticos das pesquisas que envolvem seres humanos no Brasil, projetos mais simples tramitam localmente no CEP de cada instituição de origem, enquanto projetos de áreas específicas ou mais complexos tramitam diretamente no CONEP. Existem várias legislações associadas à ética em pesquisa com seres humanos. Destacam-se a Resolução nº 466, de 12 de dezembro de 2012, sobre as normas Regulamentadoras da pesquisa envolvendo seres humanos e a Resolução nº 441 de 12 de maio de 2011 sobre as diretrizes para análise ética de projetos de pesquisa que envolvam armazenamento de material biológico humano ou uso de material armazenado em pesquisas anteriores.
Pesquisa com animais – CEUA/CONCEA
A pesquisa com uso de animais é regida por legislações próprias, e a Comissão de Ética no Uso de Animais (CEUA) é a instância institucional responsável por analisar os projetos de pesquisa que envolvam o uso de animais em atividades de pesquisa, de ensino e de treinamento. Toda instituição que crie ou utilize animais para pesquisa ou ensino, deverá requerer o credenciamento junto ao Conselho Nacional de Controle da Experimentação Animal (CONCEA), órgão do Ministério da Ciência, Tecnologia e Inovação (MCTI). A legislação pertinente é a LEI Nº 11.794, DE 8 DE OUTUBRO DE 2008, conhecida como Lei Arouca. Neste curso, vamos abordar principalmente os aspectos éticos da pesquisa com seres humanos. Contudo caso queira se aprofundar nessa temática, é possível acessar material bibliográfico pertinente.
Material complementar sobre ética no uso de animais:
Brasil. Ministério da Ciência, Tecnologia e Inovação. Conselho Nacional de Controle de Experimentação Animal. Diretriz brasileira para o cuidado e a utilização de animais em atividades de ensino ou de pesquisa científica - DBCA / Conselho Nacional de Controle de Experimentação Animal; organizadores, Márcia dos Santos Gonçalves, Antônio Américo Barbosa Viana. -- 1. ed. -- Brasília: Ministério da Ciência, Tecnologia e Inovação, 2024. 64 p. ISBN: 978-65-5471-019-0. Disponível em: https://drive.google.com/file/d/1CLmSF75tyKwDPbvI1Q4X3TUXVzvjEzoz/view?pli=1 acesso em 31/12/2024
Resumindo, na figura a seguir, uma visão esquemática do fluxo de tramitação de projetos de pesquisa envolvendo seres humanos ou uso de animais.
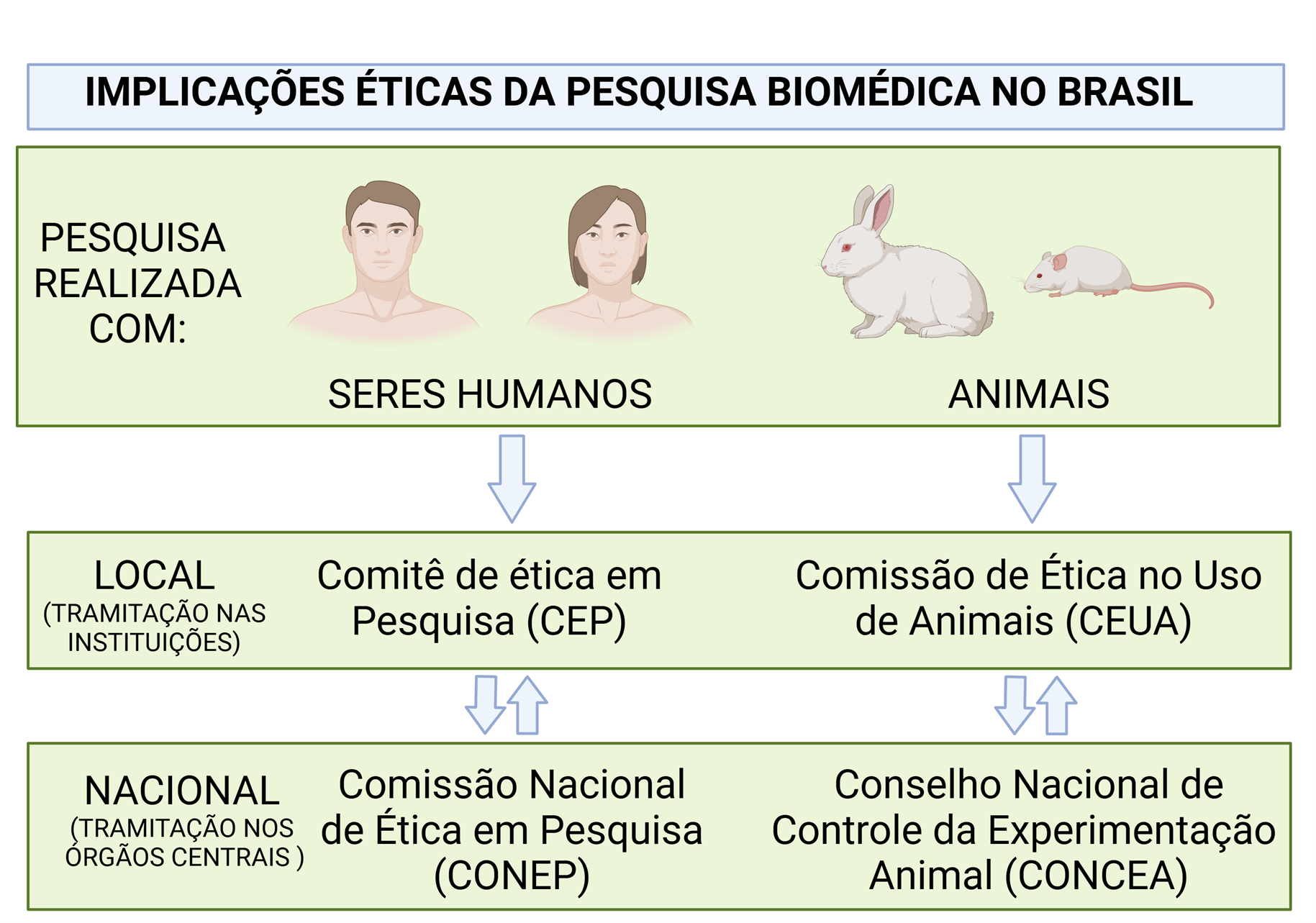
Implicações éticas em pesquisa no Brasil. A tramitação das autorizações necessárias para realização de pesquisas no Brasil, no que concerne à ética depende se a pesquisa envolve seres humanos ou animais. No caso da pesquisa com seres humanos, é feito o cadastro local na instituição de origem e ocorre a tramitação local do projeto de pesquisa no Comitê de ética em Pesquisa (CEP), em consonância com a legislação e diretrizes do órgão nacional que é a Comissão Nacional de Ética em Pesquisa (CONEP) que também realiza a análise de protocolos de pesquisa mais complexos ou de áreas específicas. Já as pesquisas envolvendo animais tramitam em suas instituições de origem na Comissão de Ética no Uso de Animais (CEUA) com coordenação nacional do Conselho Nacional de Controle da Experimentação Animal (CONCEA). Fonte: Criado em BioRender. Melo de Aguiar, A. (2024) https://BioRender.com/m029130 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: A imagem apresenta um fluxograma esquemático sobre a tramitação ética necessária para a realização de pesquisas biomédicas no Brasil, diferenciando processos para estudos com seres humanos e animais. No topo da figura, duas categorias são apresentadas: "Pesquisa realizada com:" Seres humanos (representados por ilustrações de um homem e uma mulher). Animais (representados por ilustrações de um coelho e um camundongo). Abaixo, duas setas conduzem para diferentes órgãos responsáveis pela tramitação local: Comitê de Ética em Pesquisa (CEP) para estudos com humanos. Comissão de Ética no Uso de Animais (CEUA) para estudos com animais. Na parte inferior, duas novas setas levam à tramitação nacional: Comissão Nacional de Ética em Pesquisa (CONEP) supervisiona protocolos envolvendo seres humanos. Conselho Nacional de Controle da Experimentação Animal (CONCEA) regula pesquisas com animais. O fluxo indica como as aprovações seguem um processo hierárquico, partindo do nível institucional até os órgãos reguladores nacionais.
Aspectos Legais da pesquisa com seres humanos no Brasil
No quadro comparativo a seguir, o quadro contendo informações sumarizadas sobre os documentos base da ética em pesquisa com seres humanos, e os princípios de ética em pesquisa com Seres Humanos da legislação Brasileira.
Características abordadas no documento |
Documento Base |
Legislação Brasileira |
||
Código de Nuremberg (1947) |
Declaração de Helsinki (1964) |
Relatório Belmont (1979) |
Resolução nº 466, de 12 de dezembro de 2012.
|
|
Histórico |
Código único, desenvolvido após os julgamentos de Nuremberg, em resposta aos experimentos com seres humanos conduzidos durante a Segunda Guerra Mundial. |
Feita pela Associação Médica Mundial, para preencher as lacunas do Código de Nuremberg. Com revisões periódicas a fim de atualizar |
Relatório único, Feito pela Comissão Nacional para a Proteção de Sujeitos Humanos de Pesquisa Biomédica e Comportamental motivado pelos problemas ocorridos no Estudo de Sífilis de Tuskegee (1932-1972) |
Resolução do Conselho Nacional de Saúde que versa sobre diretrizes e normas regulamentadoras das pesquisas envolvendo seres humanos |
Consentimento do participante |
Consentimento informado é essencial, consentimento por escrito (Declaração de Helsinki) |
Uso do Termo de Consentimento Livre e Esclarecido - TCLE por escrito |
||
Autonomia do participante |
Participante pode desistir a qualquer momento. |
Autonomia do participante em participar da pesquisa, por intermédio de manifestação livre e esclarecida |
||
Respeito pelo participante |
Ausência de coerção |
Cautela se o participante depende do pesquisador, diretrizes claras para grupos vulneráveis |
Respeito pelas pessoas: autonomia do participante. Os pesquisadores devem ser honestos e não omitir informações dos participantes |
Respeito à dignidade do ser humano e à autonomia do participante |
Estudo Formulado dom Rigor científico |
Estudo bem formulado e embasado cientificamente, realizado por pesquisadores habilitados |
Pesquisa precisa ser apreciada e aprovada por comitê específico |
Avaliação de riscos e benefícios |
Pesquisa deve atender aos fundamentos éticos e científicos pertinentes com submissão e aprovação prévias ao seu início pelo sistema CEP/CONEP; |
Risco benefício favorável ao participante |
Risco/benefício favorável |
Bem-estar do participante deve estar acima dos interesses da pesquisa e da sociedade. |
Beneficência: maximizar os benefícios e minimizar os riscos para os participantes da pesquisa. |
Pondera sobre o balanço de riscos e benefícios, individuais ou coletivos, visando o máximo de benefícios e o mínimo de danos e riscos; explicar os possíveis riscos aos participantes. |
Uso do Placebo |
|
Utilização limitada e controlada de placebo |
Justiça: distribuição justa de riscos e benefícios para os participantes e com igualdade. |
Justificar o uso do placebo quanto à não maleficência, aplicação metodológica, avaliação dos riscos e benefícios de um novo método terapêutico em comparação com os melhores métodos atuais disponíveis. |
Políticas quanto a banco de dados e boiamos |
|
Menção a políticas e diretrizes para estabelecimento e monitoramento de bancos de dados e Biobancos |
|
Menciona. os protocolos de formação e funcionamento de biobancos para fins de pesquisa científica; Resolução específica para o tema: Resolução 441 de 12/05/2011 |
Adaptado de: Brasil, Ministério da Saúde, Wikipedia, World Medical Association, Shuster, E. (1997), BMJ (1996)
Para saber sobre esse tema assista a nossa videoaula e acesse o texto da transcrição:






