Módulo 5TÉCNICAS BÁSICAS DE CULTIVO CELULAR
MÓDULO 5 – AULA 4 -Subcultura e Quantificação celular
Introdução
Subcultura é o procedimento de transferir células de um frasco de cultivo para outro a fim de possibilitar o crescimento celular em novas garrafas de cultura, realizando a expansão celular ou para a realização de experimentos ou procedimentos como a criopreservação. A subcultura de células aderentes é realizada quando não há mais área de crescimento celular disponível, e linhagens celulares apresentam a característica de inibir o crescimento por contato com outras células, deixam de proliferar. O processo de subcultura também é chamado de repique celular ou passagem (ATCC, 2014). A adesão as células ao substrato celular ocorre por interações eletrotáticas da superfícide crescimento celular carregada
negativamente e a interação com proteínas de adesão celular dependentes de cátions divalentes, como Ca+2 e Mg+2 , uma vez estabelecida a adesão ao substrato celular, a própria célula secreta matriz extracelular (ATCC, 2014). Os métodos de dissociação celular podem ser classificados em mecânicos ou enzimáticos:
Dentre os métodos enzimáticos a enzima proteolítica inespecífica mais utilizada é a tripsina. Essa enzima é responsável por hidrolisar cadeias polipeptídicas nos radicais lisil- arginil formando terminações de clivagem, éster e amida. Essa reação desestrutura a matriz, impossibilitando a ligação dos receptores da superfície celular, ligados ao citoesqueleto e à matriz, desta forma as células rearranjam seu citoesqueleto (ALVES; GUIMARÃES, 2010).
Os cultivos celulares não aderentes são subcultivados de forma mais simples, seja pela diluição de uma alíquota da suspensão celular em meio de cultivo novo em novos frascos de cultivo, seja pela centrifugação para remoção do meio de cultivo já utilizado e troca para meio de cultivo novo.
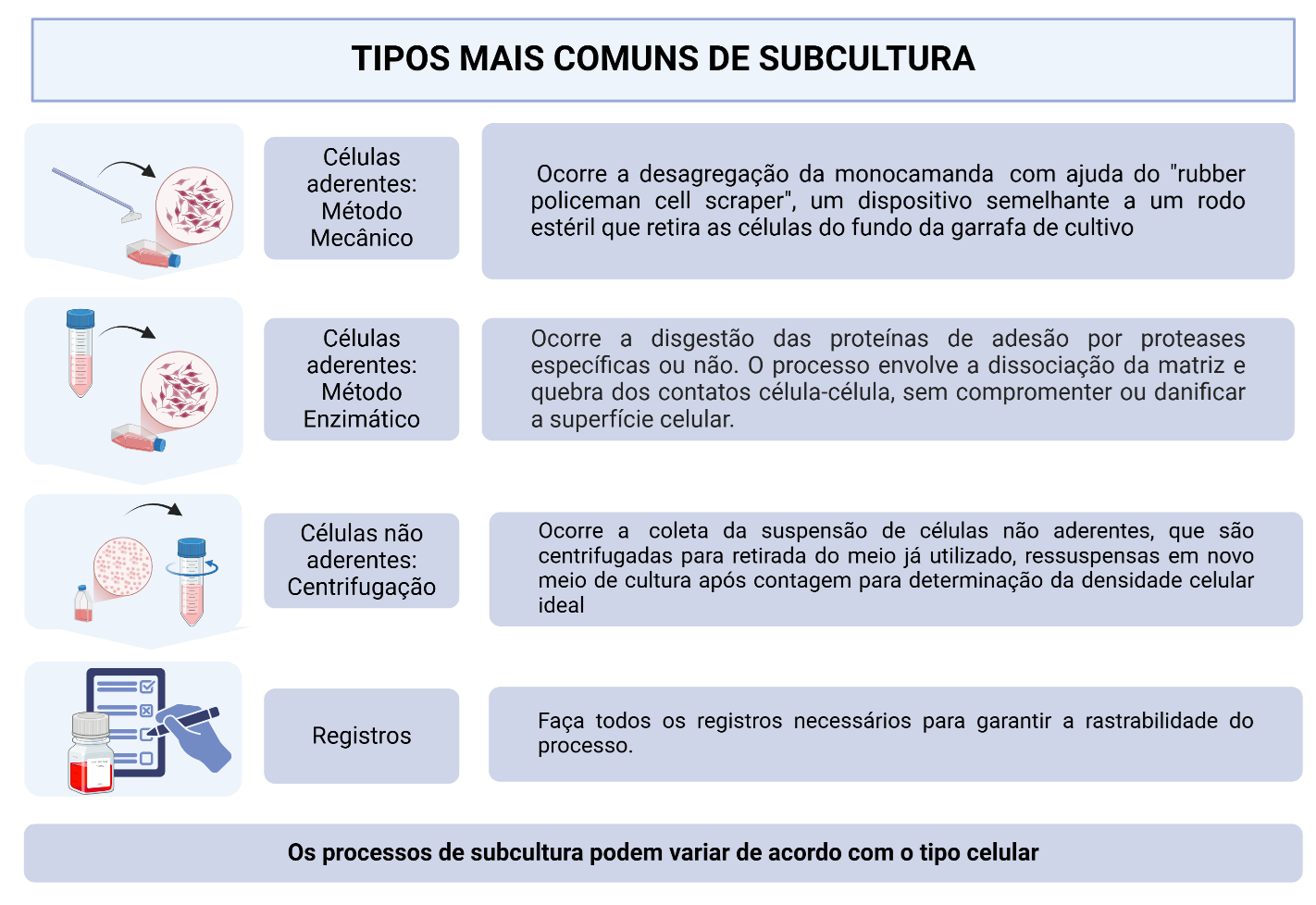
Tipos mais comuns de subcultura. Adaptado de American Type Culture Collection (2014). Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025) https://BioRender.com/b85t653. Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/).
Descrição estendida da legenda: A imagem apresenta um esquema ilustrativo dos principais métodos de subcultura utilizados para diferentes tipos de células: 1) Células aderentes – Método Mecânico: Desagregação da monocamada celular utilizando um "rubber policeman" ou cell scraper, que são dispositivos semelhantes a um rodo estéril, usados para desprender as células do fundo da garrafa de cultivo. 2) Células aderentes – Método Enzimático: Uso de enzimas, como tripsina ou colagenase, para digestão das proteínas de adesão celular. Esse processo dissocia a matriz extracelular e os contatos célula-célula sem danificar as células. 3) Células não aderentes – Centrifugação: As células suspensas são coletadas, centrifugadas para remoção do meio de cultura já utilizado e, após contagem para determinação da densidade celular, são ressuspensas em novo meio de cultura. 4) Registros: Todas as etapas do processo devem ser registradas para garantir a rastreabilidade do procedimento. E por fim, a subcultura pode variar conforme o tipo celular e os requerimentos do experimento.
Segue-se um modelo de protocolo de subcultura celular por método enzimático, o mais comum para cultivos celulares aderentes:
PROTOCOLO DE SUBCULTIVO CELULAR
Para expansão das culturas, as células aderidas ao plástico devem ser tratadas com tripsina. A atividade proteolítica da enzima age sobre as proteínas de superfície celular e resulta no desprendimento das células das garrafas de cultivo. Após esta etapa deve ser feita contagem celular na Câmara de Neubauer e verificação da viabilidade celular através do método de exclusão, utilizando o corante azul de tripan (Trypan blue), o qual penetra em células cujas membranas não estejam mais íntegras. Portanto, as células mortas são visualizadas em azul.
PROTOCOLO MODELO DE SUBCULTURA OU REPIQUE CELULAR:
Esse protocolo pode variar de acordo com procedimentos adotados em cada laboratório.
O conteúdo a seguir foi adaptado do procedimento descrito na dissertação de mestrado da autora:
KULIGOVSKI, Crisciele. Estabelecimento de banco de linhagens celulares aplicadas a pesquisa científica e ensaios toxicológicos in vitro. 2020. Dissertação (Mestrado em Engenharia Biomédica) – Universidade Tecnológica Federal do Paraná, Curitiba, 2020. Disponível em: http://repositorio.utfpr.edu.br/jspui/handle/1/24680. Acesso em 07/05/2021
- Retirar o meio de cultura;
- Adicionar solução salina balanceada livre de cálcio e magnésio (BSS.CMF) ou solução salina tamponada com fosfato (PBS) para a lavagem das culturas;
- Retirar a solução de BSS.CMF e/ou PBS e adicionar tripsina 0,05%/EDTA 0,02%;
- Observar se as células se desprenderam da garrafa, alternativamente, dependendo do tipo celular pode-se incubar as garrafas de cultura por cerca de 3-5 min a 37ºC para propiciar a individualização das células;
- Adicionar meio de cultura com SFB para parar a ação da tripsina;
- Centrifugar a 120 g por 7 min a 4ºC;
- Ressuspender o pellet de células em meio de cultura suplementado adequado a linhagem celular;
- Retirar uma alíquota de células para contar e manter o restante no gelo;
- Adicionar 10 μl do corante azul de tripano em 10 μl suspenção celular e contar em câmara de Neubauer, conforme descrito abaixo no ítem contagem celular.
- Para expansão da cultura, plaquear o número de células adequado, de acordo com a linhagem celular, algumas linhagens celulares apresentam a densidade celular ideal para plaqueamento de 2000 células/cm2
- manter as garrafas de cultivo em estufa de atmosfera úmida, 5% CO2, 37ºC.
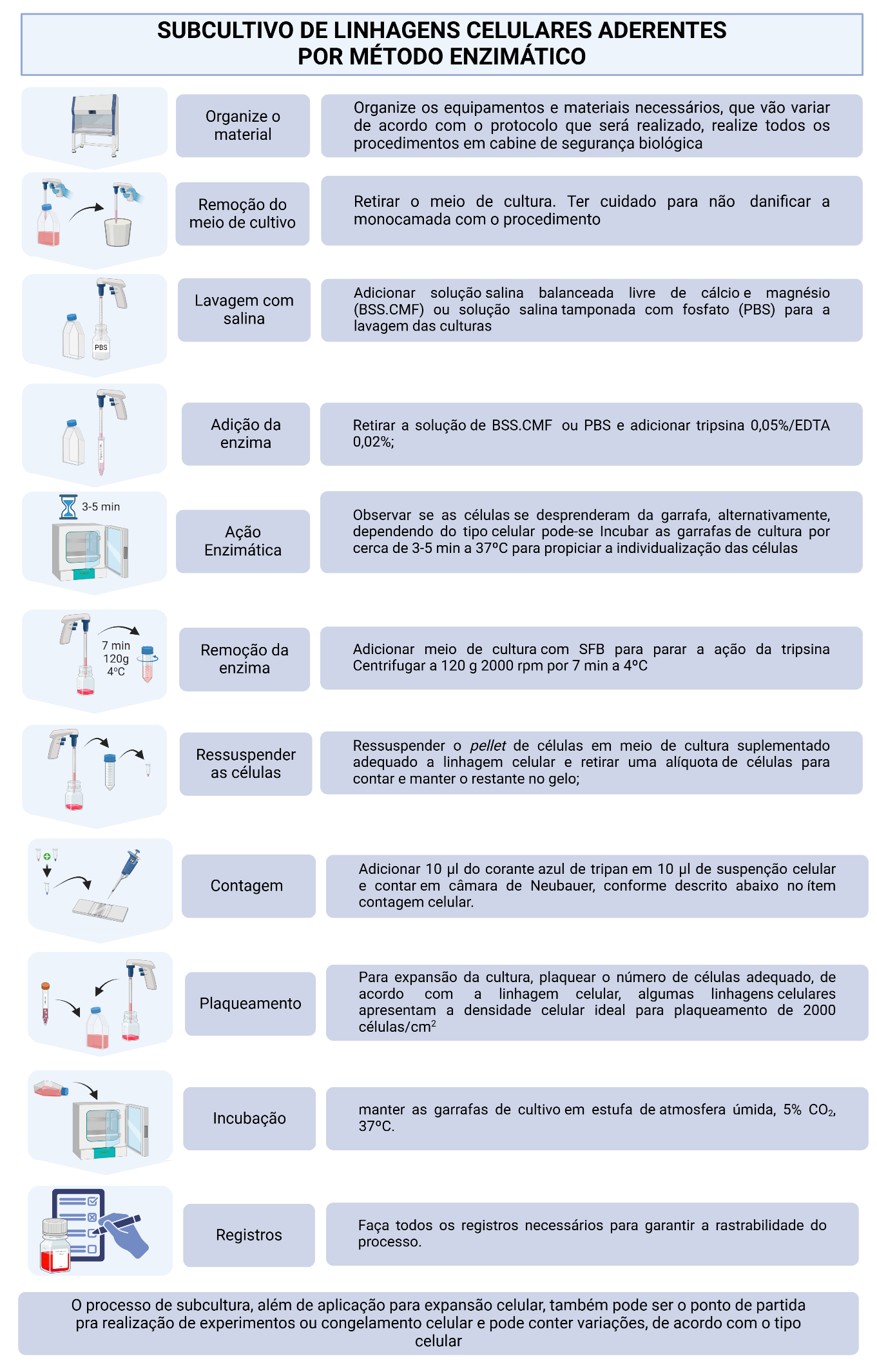
Subcultura ou repique celular de linhagens aderentes. Protocolo modelo de cultivo celular. Adaptado de American Type Culture Collection (2014). e Freshney 2010. Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025) https://BioRender.com/r04l336. Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: A figura apresenta um protocolo esquemático para o subcultivo de linhagens celulares aderentes utilizando o método enzimático, destacando todas as etapas do processo:1) Organização do material: Equipamentos e materiais são organizados, garantindo que todos os procedimentos sejam realizados em cabine de segurança biológica. 2) Remoção do meio de cultivo: O meio de cultura antigo é removido, evitando danos à monocamada celular. 3) Lavagem com solução salina: As células são lavadas com solução balanceada livre de cálcio e magnésio (BSS.CMF) ou PBS tamponado. 4) Adição da enzima: A solução de lavagem é descartada, e é adicionada tripsina 0,05% / EDTA 0,02% para desagregar as células aderentes. 5) Ação enzimática: A garrafa de cultivo é incubada por 3-5 minutos a 37°C para individualizar as células. 6) Remoção da enzima: A tripsina é neutralizada com meio de cultura contendo SFB (soro fetal bovino) e as células são centrifugadas para remoção da enzima. 7) Ressuspensão das células: O pellet celular obtido na centrifugação é ressuspendido em meio fresco adequado para a linhagem celular em estudo. 8) Contagem celular: Uma alíquota da suspensão é misturada com corante azul de tripan e contada em câmara de Neubauer para determinar a viabilidade e concentração celular. 9) Plaqueamento: Para a expansão da cultura, as células são semeadas em novas garrafas de cultivo, respeitando a densidade ideal (exemplo: 2000 células/cm²). 10) Incubação: As células são incubadas em estufa de CO2 a 37°C em atmosfera úmida. 11) Registros: Todas as etapas devem ser documentadas para garantir a rastreabilidade do processo. Em resumo, o processo de subcultura é essencial para a manutenção e expansão das linhagens celulares e pode ser ajustado de acordo com a necessidade experimental, como realização de ensaios ou congelamento celular.
Para saber sobre esse tema assista a nossa videoaula e acesse o texto da transcrição:
Saiba mais em conteúdos do curso: No módulo de meio de cultivo e substratos celulares é possível ver as características dos principais suplementos utilizados em cultivos celulares.
QUANTIFICAÇÃO CELULAR
Durante o subcultivo celular, as células devem ser quantificadas de forma a permitir que a quantidade adequada de células seja repassada para garrafas de cultura ou plaqueadas para experimentos e também conhecer a viabilidade celular. As células podem ser quantificadas de forma simples, por contagem direta da suspensão celular em câmaras próprias de contagem, com áreas delimitadas por quadrantes ou regiões de dimensões conhecidas, onde é possível fazer uma associação entre o número de células contato e a concentração celular por volume. As câmaras de Neubauer (3x3 mm x 0,1 mm de profundidade) são feitas de vidro e possuem duas zonas de contagem (câmara superior e inferior) separadas por um sulco horizontal e limitadas de cada lado por um canal vertical, conforme figura abaixo. Para que se crie um espaço que possa ser preenchido por um determinado volume, coloca-se uma lamínula sobre as zonas de contagem da câmara, formando-se um espaço com uma altura de 0,1 mm. A superfície de contagem, quadriculada, está marcada com um grande quadrado que tem 3 mm de lado.
Relembrando o conteúdo já apresentado sobre câmara de Neubauer no módulo sobre estrutura equipamentos em laboratórios de cultivo celular:
Camara de Neubauer. Características, aplicações e cuidados. Imagem representativa dos quadrantes de uma Câmara de Neubauer utilizada para quantificação de células em suspensão.Adaptado de Freshney, 2010 Fonte: Criado em BioRender.Melo de Aguiar, A. & Souza, A, C, G. (2025) https://BioRender.com/c68y812 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda:A imagem apresenta uma Câmara de Neubauer, um equipamento de vidro utilizado para quantificação de células em suspensão. A câmara possui um sistema de grade com 9 quadrantes principais, cada um com 1 mm² de área, permitindo a contagem precisa de células. Estrutura e funcionamento: A câmara possui duas áreas de contagem, separadas por um sulco horizontal e limitadas lateralmente por canais verticais. Cada câmara contém quatro zonas de contagem para melhor distribuição da amostra. Aplicações: Utilizada para definir a concentração celular em suspensão, geralmente em conjunto com corantes vitais como o Azul de Tripan, permitindo a análise da viabilidade celular. Cuidados: Para preservar a integridade da câmara, recomenda-se secar com papel macio e não abrasivo e realizar a limpeza e desinfecção adequadas após cada uso, garantindo a precisão das contagens.
A quantidade de células que serão repassadas para garrafas ou placas de cultivo depende do tipo celular e também do experimento a ser realizado. Por exemplo, algumas linhagens celulares, é indicado utilizar 2000 células/cm². Dessa forma, a quantidade final de células varia de acordo com o tamanho da garrafa, como pode ser observado na tabela abaixo:
Tabela 1: Quantidade de células necessárias para expansão celular com densidade celular de 2000 células/cm² em garrafas de cultivo de diferentes tamanhos.
Tamanho da garrafa |
Quantidade de células |
Total de células |
T25 (25 cm²) |
2000 células/cm² |
50,000 |
T75 (75 cm²) |
2000 células/cm² |
150,000 |
T150 (150 cm²) |
2000 células/cm² |
300,000 |
Fonte: as autoras (2021).
PROTOCOLO MODELO DE QUANTIFICAÇÃO CELULAR
Esse protocolo pode variar de acordo com procedimentos adotados em cada laboratório.
O conteúdo a seguir foi adaptado do procedimento descrito na dissertação de mestrado da autora:
KULIGOVSKI, Crisciele. Estabelecimento de banco de linhagens celulares aplicadas a pesquisa científica e ensaios toxicológicos in vitro. 2020. Dissertação (Mestrado em Engenharia Biomédica) – Universidade Tecnológica Federal do Paraná, Curitiba, 2020. Disponível em: http://repositorio.utfpr.edu.br/jspui/handle/1/24680. Acesso em 07/05/2021.
- Prepare a câmara de Neubauer: umedeça os lados esmerilados com água e coloque a lamínula;
- Com uma micropipeta adicionar 10 μl do corante azul de tripan em 10 μl de células;
- Adicione 10 μl da mistura de células e azul de tripan em um dos lados da câmara, junto à lamínula em volume necessário para ocupar a região de contagem por difusão, não se deve forçar volume excessivo pois reduz a precisão da contagem;
- Coloque a câmara no microscópio;
- Conte as células vivas (não coradas em azul) e as células mortas (coradas em azul) nos 4 quadrantes (1, 2, 3 e 4) usando o microscópio;
- Calcule a concentração de células vivas na suspensão fornecida:
- Plaquear a quantidade de células necessárias de acordo com o experimento a ser conduzido. Manter as garrafas ou placas em estufa de atmosfera úmida, 5% CO2, 37ºC.
Para saber sobre esse tema assista a nossa videoaula e acesse o texto da transcrição:
Saiba mais em conteúdos do curso: No módulo de estrutura laboratorial e equipamentos é possível conhecer mais caracteristicas da câmara de neubaer, utilizada para contagem celular.






