Módulo 04 | Aula 2 Qualidade na pesquisa clínica
Sistema de Gestão de Qualidade
Um Sistema de Gestão da Qualidade (SGQ) em pesquisa clínica é um conjunto de políticas, procedimentos e práticas documentadas que são implementadas para garantir a qualidade e a conformidade dos processos relacionados à pesquisa clínica. Veja uma representação gráfica do SGQ:
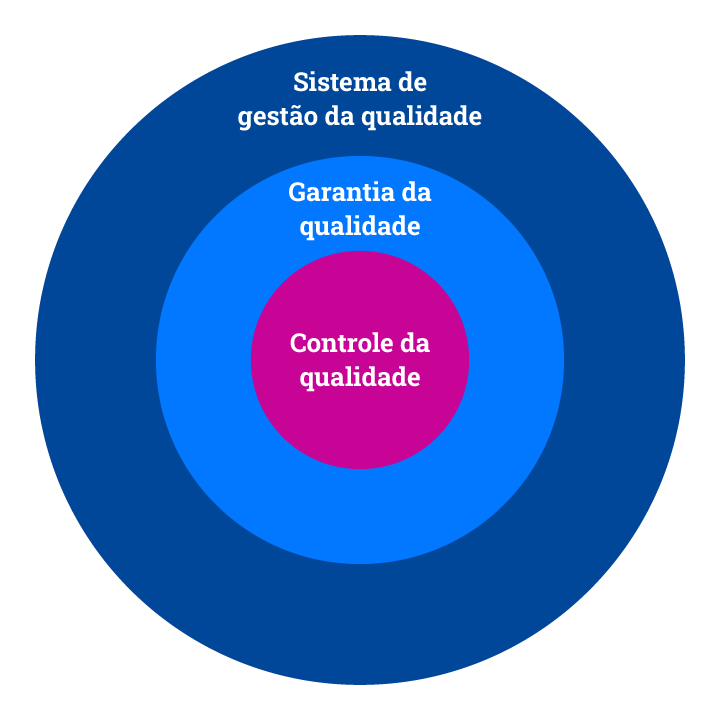
A seguir, conheça alguns componentes-chave de um SGQ em pesquisa clínica.
Desenvolvimento e documentação de políticas claras que estabeleçam os princípios e diretrizes gerais para a condução de pesquisas clínicas, e elaboração de procedimentos detalhados que descrevem as etapas específicas a serem seguidas em todas as fases do estudo, desde o planejamento até a conclusão e relato dos resultados.
Fornecimento de treinamento adequado para todos os membros da equipe envolvidos na pesquisa clínica, incluindo pesquisadores, coordenadores de pesquisa, pessoal de laboratório, farmácia e outros profissionais. Além disso, estabelece critérios de qualificação e competência para garantir que os membros da equipe tenham o conhecimento e as habilidades necessárias para desempenhar suas funções de forma eficaz.
Implementação de um sistema robusto para controlar e revisar documentos essenciais, como protocolos de pesquisa, formulários de coleta de dados, relatórios de monitoramento e registros de consentimento livre e esclarecidos (TCLE / RCLE). Também inclui a manutenção de registros precisos e atualizados de todas as atividades relacionadas à pesquisa clínica, contendo comunicações, decisões e desvios identificados.
Realização de monitoramento regular do estudo para garantir o cumprimento dos protocolos de pesquisa, regulamentos aplicáveis e boas práticas clínicas, e condução de auditorias internas e externas para avaliar a conformidade do estudo com os requisitos regulatórios e a integridade dos dados coletados.
Identificação proativa de potenciais riscos e desvios que possam afetar a qualidade e a integridade dos dados do estudo. Igualmente, o desenvolvimento e a implementação de estratégias de mitigação de riscos a fim de minimizar a ocorrência de problemas durante a condução do estudo. Você verá mais detalhes sobre esse componente a seguir.
Gerenciamento de Riscos
O gerenciamento de riscos na pesquisa clínica é uma prática fundamental para identificar, avaliar e mitigar os riscos potenciais que podem afetar a integridade dos dados, a segurança dos participantes e o sucesso do estudo. Aqui estão os principais aspectos do gerenciamento de riscos na pesquisa clínica:
pan_tool_alt Clique Toque nos botões para visualizar as informações.
Além disso, existem outros aspectos que devem ser considerados, que são:
Em resumo, o gerenciamento de riscos na pesquisa clínica é uma prática essencial para garantir a segurança dos participantes, a integridade dos dados e o sucesso geral do estudo. Ao identificar, avaliar e mitigar os riscos potenciais de forma proativa, os pesquisadores podem minimizar as incertezas e aumentar a confiabilidade dos resultados do estudo.
Melhoria Contínua
O processo de melhoria contínua consiste no estabelecimento de mecanismos para avaliar e revisar regularmente os processos do SGQ, com o objetivo de identificar oportunidades de melhoria e implementar mudanças que promovam eficiência e qualidade.
Um SGQ eficaz em pesquisa clínica é essencial para garantir a integridade dos dados, a segurança dos participantes do estudo e conformidade com os requisitos regulatórios, contribuindo assim para a credibilidade e a confiabilidade dos resultados da pesquisa. Conheça agora algumas atividades que fazem parte do processo de melhoria contínua.
Define como os processos de controle e garantia de qualidade serão cumpridos durante todo o ensaio clínico e descreve várias tarefas relacionadas à qualidade no estudo. Ele documenta práticas de qualidade, recursos e atividades que são específicas para um projeto.
A partir da terceira revisão do Guia de Boas Práticas Clínicas, foi incorporado o conceito de Quality by Design, que estabelece o seguinte: a qualidade deve ser implementada desde a concepção do estudo clínico, de modo a identificar os riscos associados aos processos e dados , além de estabelecer formas de mitigação.
Um dos pontos considerados nessa abordagem é a construção de um desenho de estudo o mais simples possível, com fácil logística e evitando complexidades desnecessárias. Além disso, essa abordagem envolve a identificação de fatores críticos para a qualidade, a gestão de riscos associados a esses fatores e a implementação de medidas para garantir que os objetivos do estudo sejam alcançados. O foco passa de detecção reativa de problemas para prevenção proativa de erros que possam impactar a segurança dos participantes ou a confiabilidade dos dados.



