Módulo 2Isolamento e Purificação Celular
MÓDULO 2 – AULA 1 - Isolamento e Biologia das células animais em cultura
Como é possível obter as células para estabelecimento das culturas?
Os tecidos de animais constituem a fonte primária de células para cultura celular. Essas células podem ser isoladas através de diferentes metodologias e uma vez cultivadas originam as culturas primárias (período que antecede o primeiro subcultivo). Em geral, essas células apresentam capacidade proliferativa limitada devido à aquisição de senescência replicativa após algumas dezenas de passagens na cultura, com exceção de células obtidas a partir de tumores. Eventualmente, as células cultivadas podem sofrer imortalização natural ou induzida, estabelecendo as linhagens celulares.
O que é senescência replicativa?
As células somáticas apresentam capacidade proliferativa limitada. Na maioria das células conhecidas isso se deve a não expressão do gene que codifica para a enzima telomerase. Sem a telomerase, não há extensão do final dos cromossomos lineares para a síntese de DNA, de modo que os telômeros diminuem de tamanho em cada ciclo de replicação do DNA. Quando atingem um tamanho crítico, sistemas de reparo do DNA iniciam eventos que culminam com anomalias cromossômicas que levam ao bloqueio do ciclo celular. Algumas células não sofrem senescência, pois expressam naturalmente a enzima telomerase (células-tronco e que originam gametas) ou voltam a expressá-la (células cancerosas e de linhagens celulares imortalizadas).
Como é a Biologia das células em cultura?
A transferência das células da situação in vivo para o ambiente in vitro em cultura envolve mudanças que afetam significativamente características das células.
As células no ambiente in vivo / organismo:
- Estão organizadas em tecidos que apresentam uma arquitetura tridimensional característica.
- Normalmente interagem fisicamente com diferentes tipos celulares, muitas vezes de diferentes tecidos.
- Interagem com fatores e moléculas sinalizadoras bastante diversificadas (p.ex., hormônios, citocinas, neurotransmissores), algumas produzidas em sítios distantes do organismo.
- São mantidas em condições particulares de temperatura, pressão parcial de O2 e CO2, e às vezes, interfaces características nos domínios basal e apical das células (p.ex., fluido extracelular/ar, lâmina basal/domínio basal de outras células).
- Estão sujeitas a uma interação sistêmica muito complexa que modula sua atividade metabólica, grau de diferenciação, proliferação etc.
As células no ambiente in vitro / em cultura:
- Normalmente são mantidas em monocamadas (culturas 2D), embora possam também ser cultivadas em arranjos tridimensionais mais complexos (culturas 3D).
- Não interagem com tipos de células diferentes, exceto quando em coculturas.
- Estão sujeitas apenas aos fatores produzidos por outras células em cultura ou supridos via meio de cultura, o que pode afetar o seu fenótipo.
- São mantidas sob baixa concentração de O2 no meio de cultura, e na maioria dos casos, alta pressão parcial de CO2, o que altera seu metabolismo energético (há aumento da dependência das células da glicólise para suprir ATP).
- Normalmente são cultivadas em monocamadas, com domínio basal sobre moléculas de matriz extracelular (que estão aderidas ao frasco de cultura) e domínio apical banhado por meio de cultura.
- São mantidas em condições bastante controladas, sem interações sistêmicas complexas, de modo que pode haver alterações fenotípicas relevantes como mudanças metabólicas e grau de diferenciação (p.ex., alteração nos níveis de expressão de moléculas características do tipo celular), alterações na proliferação (p.ex., incapacidade de proliferação sob determinadas condições de cultura para alguns tipos celulares ou indução de proliferação em outros).
Características |
Células no ambiente |
Células no ambiente |
Arquitetura celular |
Tecidos com arquitetura tridimensional característica. |
Monocamadas (culturas 2D) ou arranjos tridimensionais mais complexos (culturas 3D). |
Interação celular |
Interações heterotípicas com diferentes tipos celulares, frequentemente de tecidos distintos. |
Não interagem com tipos celulares diversos, exceto em coculturas. |
Interação com fatores e moléculas |
Fatores diversificados (hormônios, citocinas, neurotransmissores), incluindo moléculas produzidas em sítios distantes, adaptações à respostas fisiológicas. |
Interagem apenas com fatores presentes no meio de cultura ou produzidos por outras células em cultura, o que pode afetar o fenótipo celular. |
Condições físicas e químicas |
Mantidas em condições específicas de temperatura, pressão parcial de O₂ e CO₂, além de interfaces basais e apicais características. |
Cultivadas sob baixa concentração de O₂ e alta pressão parcial de CO₂, com domínio basal em matriz extracelular (aderidas ao frasco) e domínio apical banhado por meio de cultura. |
Complexidade sistêmica |
Sujeitas a interações sistêmicas complexas que modulam metabolismo, diferenciação, proliferação e outras funções celulares. |
Mantidas em condições controladas, sem interações sistêmicas, resultando em alterações fenotípicas (ex.: metabolismo, grau de diferenciação e proliferação). Sistemas de microfluídica buscam contribuir para uma maior complexidade dos modelos a fim de maior aproximação com a fisiologia de organismos |
Metabolismo energético |
Influenciado por interações sistêmicas e condições locais do tecido. |
Dependem mais da glicólise para produção de ATP, devido às condições típicas de cultivo com baixa concentração de O₂ e alta pressão parcial de CO₂. |
Controle experimental |
Difícil de controlar, dada a alta complexidade e variabilidade entre organismos. |
Condições altamente controladas, com possibilidade de replicar experimentos com maior precisão. |
Simulação de microambientes |
Microambientes específicos ocorrem naturalmente devido à arquitetura e organização dos tecidos. |
Microambientes podem ser simulados utilizando scaffolds, biomateriais ou sistemas 3D, bioimpressão, etc para minetizar características do ambiente in vivo, incluindo modelos de microfluídica. |
Diversidade celular |
Inclui uma vasta diversidade de tipos celulares interagindo em um organismo completo. |
Pode incluir apenas um tipo celular ou tipos limitados em coculturas. |
Tempo de manutenção |
As células permanecem no organismo enquanto ele está vivo, com autorrenovação em certos casos. |
Culturas são mantidas por períodos limitados e necessitam de subcultivo regular para evitar senescência ou confluência excessiva, ou podem ser preservados através de procedimentos de criopreservação. |
Condições de esterilidade |
Organismos têm sistemas naturais de defesa contra contaminantes, mas estão sujeitos a infecções. |
Culturas celulares requerem condições rigorosamente estéreis para evitar contaminações por fungos, bactérias e micoplasma. |
Substrato de crescimento |
Crescem naturalmente em matriz extracelular e interagem com componentes endógenos. |
Dependem de substratos artificiais, como frascos ou placas de cultura recobertas com matriz extracelular artificial (p.ex., colágeno, fibronectina). |
Comparativo características das células em ambientes in vivo e in vitro são sumarizados no quadro abaixo (Adaptado de Freshney, 2010):
Etapas para o isolamento de células
1. Obtenção de autorização de comitê de ética: todo trabalho de pesquisa que envolva o uso de animais ou humanos deve ser previamente avaliado e aprovado por comitê de ética competente. Esse tema será estudado em outro módulo.
2. Aquisição da amostra: o órgão ou tecido de interesse deve ser obtido em condições assépticas a partir de tecidos ou amostras de origem animal ou humana.
3. Isolamento do(s) tecido(s): o material deve ser dissecado, na medida do possível, para a remoção de tecido necrótico, adiposo ou outros que não o de interesse, de acordo com o objetivo do isolamento celular.
4. Dissecção ou desagregação: na maioria dos casos o material deve ser cortado em pequenos fragmentos, com instrumentos apropriados e afiados para minimizar danos às células, e então seguir para cultura (explante de fragmentos de tecido) ou para desagregação das células (mecânica e/ou enzimática).
5. Cultivo: os fragmentos de tecido ou células isoladas devem ser lavados e cultivados em meio de cultura apropriado em frascos de cultura que facilitem a adesão celular*. *Com exceção de alguns tipos celulares como células hematopoiéticas e algumas células tumorais, a maioria das células precisa aderir para sobreviver em cultura.
Métodos para o isolamento de células
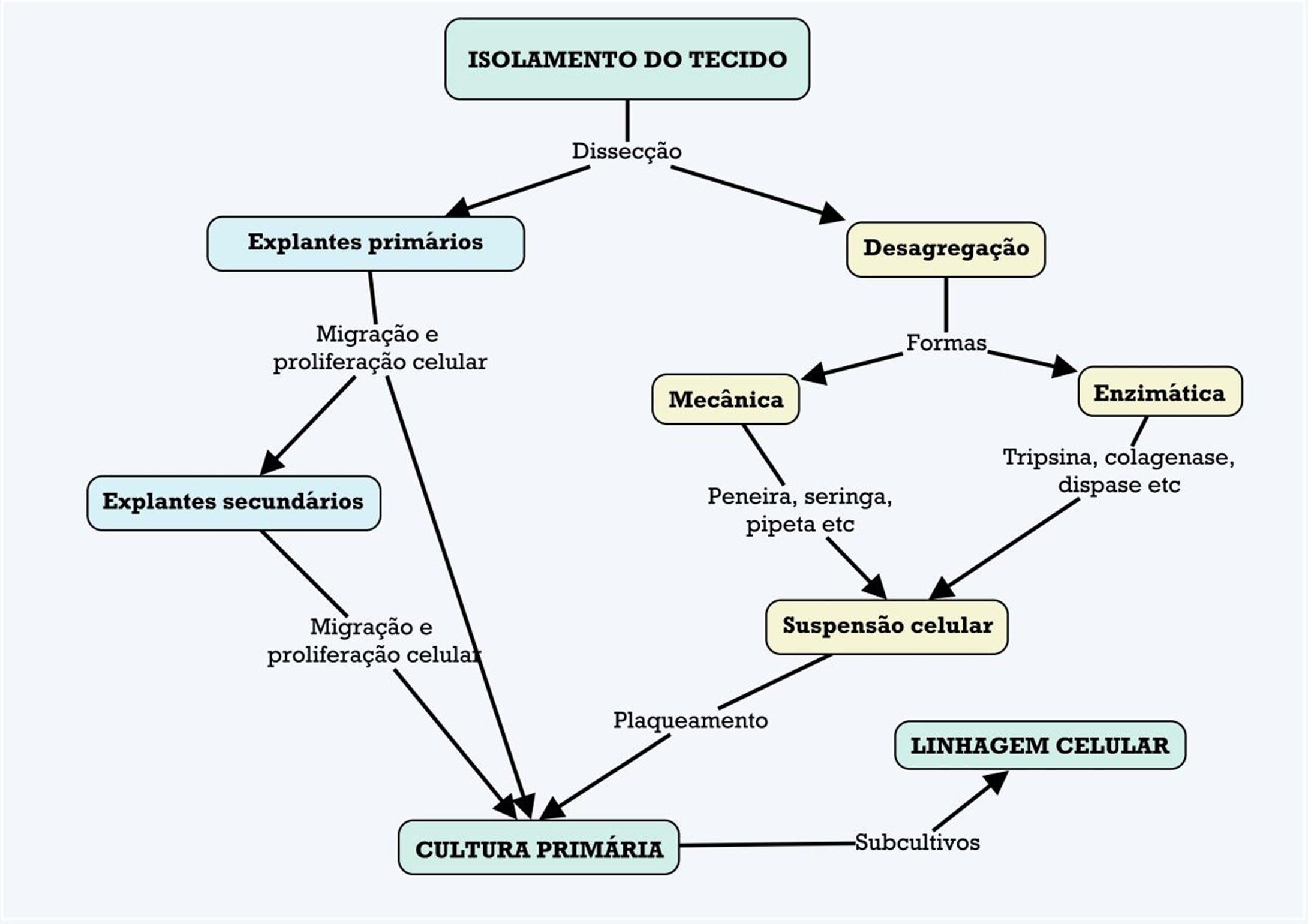
Métodos para o isolamento de células a partir de tecidos e órgãos animais. Adaptado de Freshney, 2010. Fonte: o Autor, Francisco Filipak Neto. Descrição estendida da legenda: Fluxograma ilustrando os métodos de isolamento de células a partir de tecidos e órgãos animais. O processo inicia com a dissecação do tecido, seguida por dois caminhos: cultivo de explantes primários, que podem gerar explantes secundários e evoluir para cultura primária; ou desagregação celular, que pode ser realizada por métodos mecânicos, como peneira e pipeta, ou enzimáticos, utilizando tripsina, colagenase e dispase. A desagregação gera uma suspensão celular que, após plaqueamento, pode originar uma cultura primária ou evoluir para uma linhagem celular após subcultivos. Fonte: o Autor
Isolamento celular pela técnica do explante
- Envolve o cultivo de fragmentos de tecido (1-2 mm3) dos quais células da borda migram e proliferam em cultura.
- A formação de filme de moléculas de matriz extracelular (p.ex. colágeno) no fundo do frasco de cultura pode facilitar a adesão do explante e das células.
- Após 5-7 dias já é possível verificar migração significativa de células ao redor dos explantes.
- Muitas vezes, os explantes podem ser reutilizados!
- Vantagens: útil para amostras escassas de tecidos e de fácil execução.
- Desvantagens: favorece o isolamento das células com maior capacidade de migração e proliferação; processo relativamente lento para obtenção das células isoladas e com baixo rendimento inicial quando comparado à desagregação de tecidos.
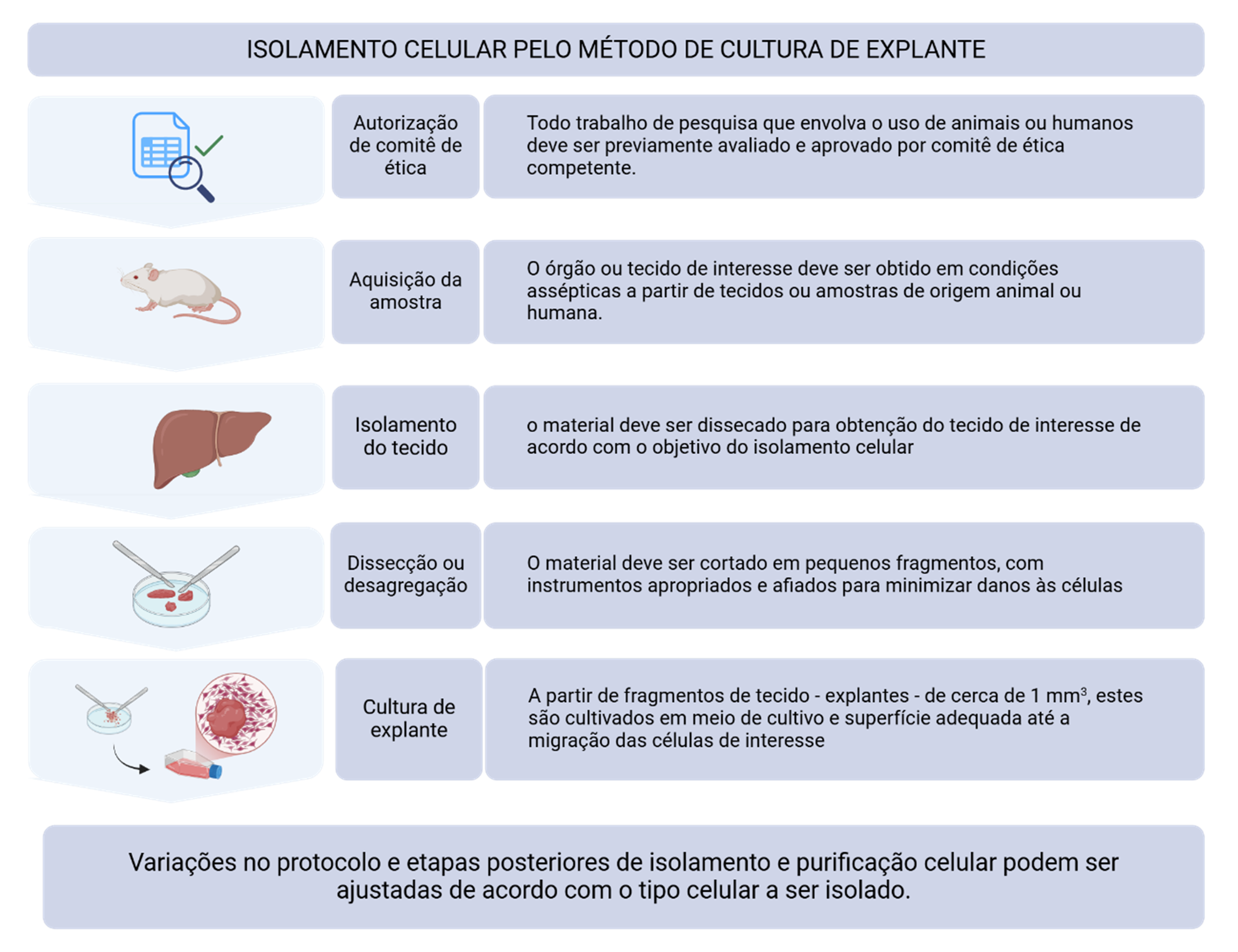
Visão esquemática do isolamento celular por cultura de explante. Todo o isolamento celular inicia com a etapa de submissão e autorização pelo comitê de ética competente de acordo com tecido de origem, se de origem humana ou animal. Segue-se então etapas de obtenção do tecido, isolamento do tecido de interesse e dissecção ou desagregação tecidual em pequenos fragmentos de cerca de 1mm3 denominado explante, que pode então ser colocado em frasco de cultivo com meio de cultivo e substrato celular adequados ao isolamento do tipo celular de interesse. Após alguns dias, se o procedimento de isolamento celular é bem sucedido, é possível observar a migração celular a partir do explante. Fonte: Criado em Biorender. Melo de Aguiar, A., Barisón, M.J. (2025) https://BioRender.com/j85n347 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: O infográfico detalha o processo de isolamento celular utilizando o método de cultura de explante, que envolve diversas etapas essenciais para obtenção de células viáveis a partir de tecidos. O fluxo inicia com a autorização do comitê de ética, garantindo que toda pesquisa com células de origem animal ou humana esteja em conformidade com as normas éticas. Em seguida, a aquisição da amostra é realizada de forma asséptica para evitar contaminações por microrganismos. Na etapa de isolamento do tecido, o material de interesse é separado do órgão ou estrutura original, permitindo que apenas o tecido relevante seja utilizado. A dissecção ou desagregação é feita com instrumentos apropriados para minimizar danos celulares e garantir a integridade dos fragmentos. Por fim, a cultura de explante consiste no cultivo dos fragmentos de tecido (explantes) em condições adequadas, permitindo que as células migrem para o meio de cultura. Esse processo pode levar alguns dias e, quando bem-sucedido, resulta na obtenção de células isoladas para estudos subsequentes. O esquema destaca que as etapas posteriores podem variar de acordo com o tipo celular a ser isolado. Variações no protocolo ou etapas subsequentes de isolamento e purificação celular podem ser ajustadas de acordo com o tipo celular a ser isolado.
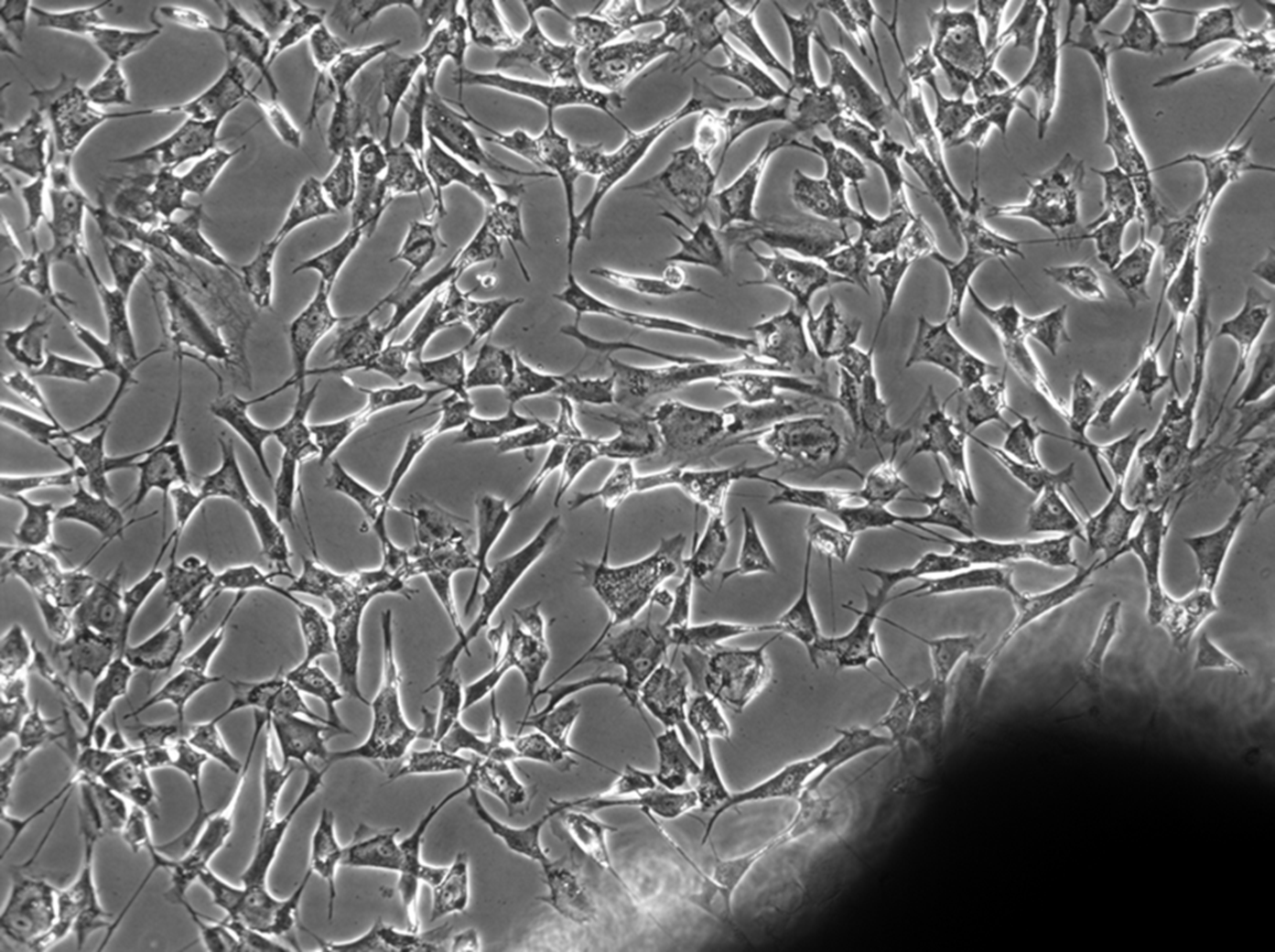
Células migrando de um fragmento de tecido cardíaco. Descrição estendida da legenda: A imagem de microscopia exibe células migrando a partir de um fragmento de tecido cardíaco, evidenciando o processo de cultura de explante. As células apresentam morfologia alongada e se espalham a partir da borda do tecido, demonstrando adesão e crescimento na superfície de cultivo. Esse método é frequentemente utilizado para isolamento celular e estudos de comportamento celular em condições controladas. FONTE: A autora (Aguiar, AM, 2011, tese de doutorado). FONTE: A autora (Aguiar, AM, 2011, tese de doutorado).
Desagregação mecânica
- Envolve o isolamento de células por ação mecânica pela fragmentação dos tecidos ao cortar, pressionar contra uma tela ou peneira, ou forçar através de uma seringa ou pipeta.
- Vantagens: processo rápido e de fácil execução para obtenção de suspensões celulares; relativamente eficiente para tecidos moles (baço, cérebro, alguns tumores e fígado embrionário).
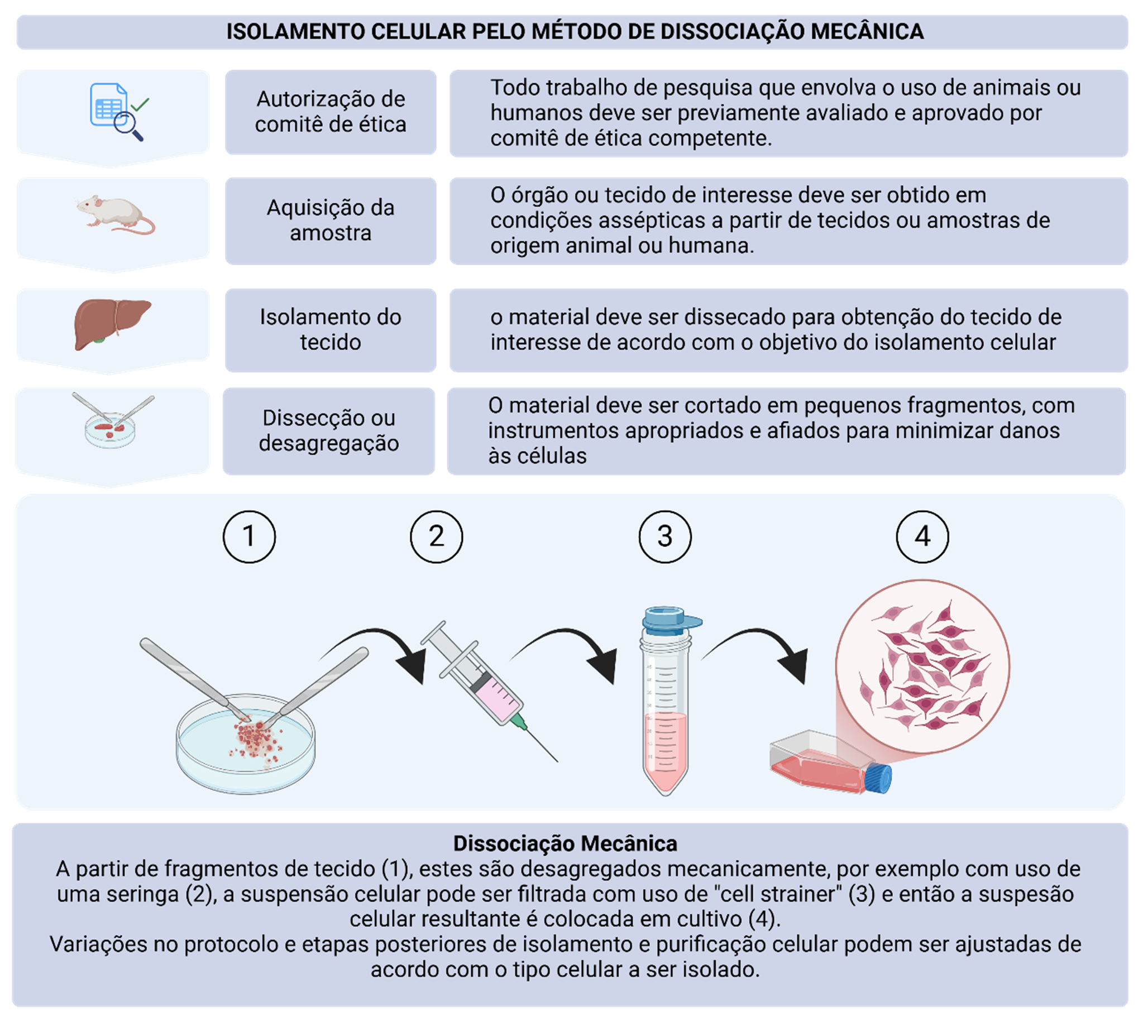
Visão esquemática do isolamento celular por dissociação mecânica. Todo o isolamento celular inicia com a etapa de submissão e autorização pelo comitê de ética competente de acordo com tecido de origem, se de origem humana ou animal. Segue-se então etapas de obtenção do tecido, isolamento do tecido de interesse e dissecção ou desagregação tecidual (etapa 1), a partir da qual os fragmentos podem ser dissociados mecanicamente com uso de uma seringa (etapa 2), que pode seguir para uma etapa de filtração em filtro do tipo “cell strainer” (etapa 3) e então a suspensão celular resultante é colocada em frasco de cultivo com meio de cultivo e substrato celular adequados ao isolamento do tipo celular de interesse (etapa 4). Após alguns dias, se o procedimento de isolamento celular é bem-sucedido, é possível células aderidas ao substrato celular. Adaptado de Freshney, 2010. Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J., (2025) https://BioRender.com/s82x166 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: Variações no protocolo ou etapas subsequentes de isolamento e purificação celular podem ser ajustadas de acordo com o tipo celular a ser isolado.
Desagregação enzimática
- Envolve a perfusão de órgãos (p.ex., fígado) e /ou incubação de fragmentos de tecido na presença de enzimas que clivam moléculas da matriz extracelular, desestabilizando a estrutura dos tecidos, e assim soltando as células.
- Pode envolver uso de quelantes de metais divalentes como o cálcio (p.ex., EDTA, EGTA) antes ou conjuntamente com a incubação com proteases (p.ex., tripsina, pronase, colagenase, dispase), bem como o uso de misturas de enzimas e/ou enzimas auxiliares (p.ex., hialuronidase, heparinase, DNAse). Isso aumenta a eficiência, visto que a adesão célula-célula e célula-matriz extracelular depende, respectivamente, da ação de caderinas e integrinas, e ambas as proteínas dependem de cálcio para atuar.
- Diferenças no tipo e grau de pureza das enzimas, temperatura e tempo de incubação afetam o rendimento e viabilidade das células isoladas. Em geral, as enzimas precisam ser removidas ou inativadas após ação para minimizar danos às células.
- Vantagens: procedimento relativamente rápido, com alto rendimento de células viáveis que melhor representam um órgão ou tecido (sem seleção, pelo menos num primeiro momento, apenas das células com maior capacidade migratória ou proliferativa).
- Desvantagens: incubações mais prolongadas e/ou uso de enzimas com menor grau de pureza aumentam o rendimento, mas também aumentam o dano às proteínas de superfície celular (p.ex., receptores) e às células mais sensíveis do tecido; procedimento mais complexo que o explante e desagregação mecânica e de maior custo.
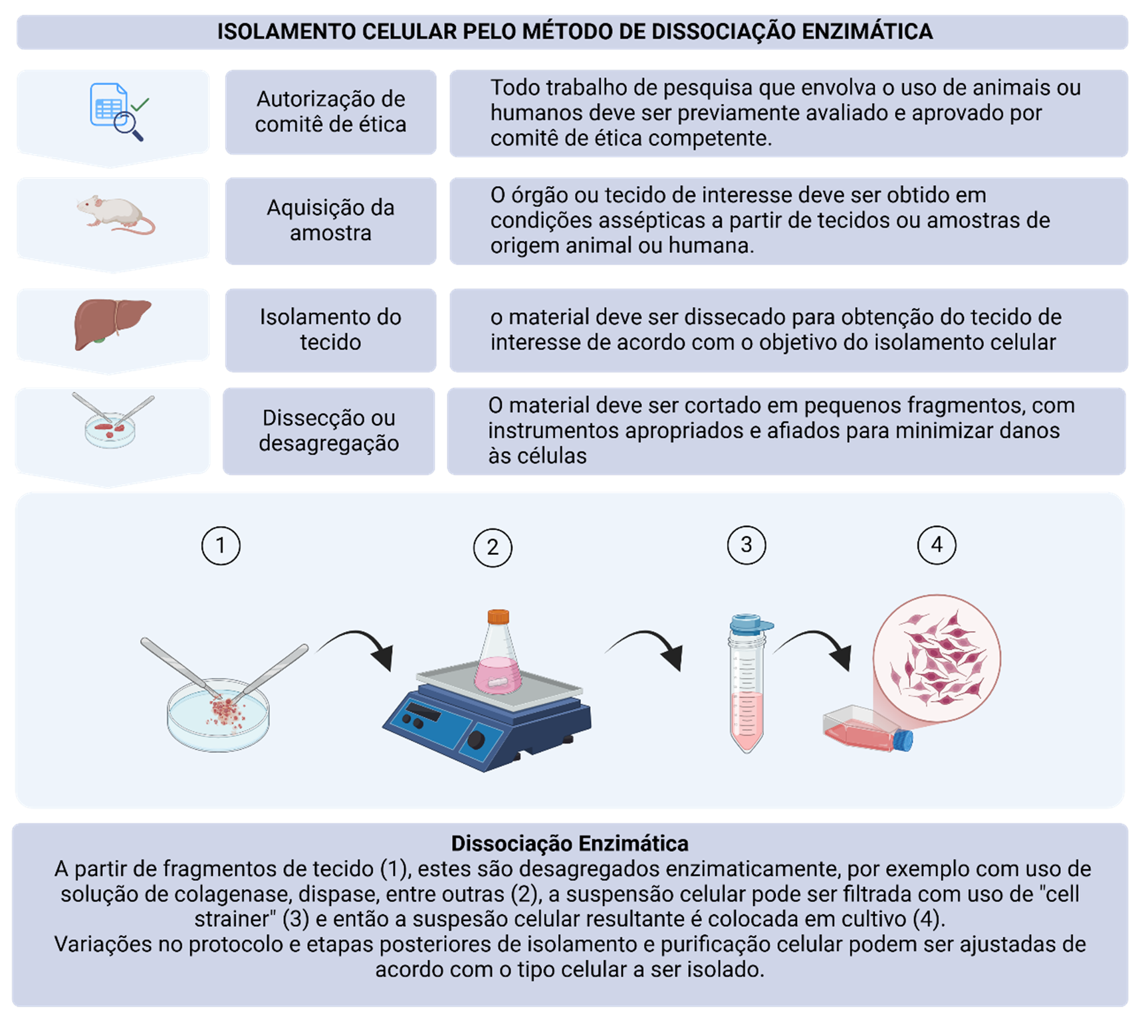
Visão esquemática do isolamento celular por dissociação enzimática. Todo o isolamento celular inicia com a etapa de submissão e autorização pelo comitê de ética competente de acordo com tecido de origem, se de origem humana ou animal. Segue-se então etapas de obtenção do tecido, isolamento do tecido de interesse e dissecção ou desagregação tecidual em pequenos fragmentos de cerca de 1mm3 denominado explante. A partir de fragmentos de tecido (etapa 1), estes são desagregados enzimaticamente, por exemplo com uso de solução de colagenese, dispase, entre outras (etapa 2), a suspensão celular pode ser filtrada com uso de "cell strainer" (etapa 3) e então a suspensão celular resultante é colocada em cultivo (etapa 4). Após alguns dias, se o procedimento de isolamento celular é bem-sucedido, é possível observar a migração celular a partir do explante. Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025) https://BioRender.com/r98z802 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: Variações no protocolo ou etapas subsequentes de isolamento e purificação celular podem ser ajustadas de acordo com o tipo celular a ser isolado.

Desagregação enzimática de células hepáticas de peixe. Após anestesia, eutanásia e assepsia do peixe, o fígado foi removido, perfundido com solução de PBS-EDTA e tripsina-EDTA, cortado em pequenos pedaços sobre uma tela de aço. Após centrifugação e lavagens em PBS e meio de cultura, pellets de células foram obtidos e cultivados. FONTE: o Autor (Filipak Neto, 2007). Descrição estendida da legenda: Sequência de imagens fotográficas ilustrando o processo de desagregação enzimática de células hepáticas de peixe. As etapas incluem anestesia, eutanásia e assepsia do peixe, seguida pela remoção do fígado, que é perfundido com solução PBS-EDTA e tripsina-EDTA. O tecido hepático é então cortado em pequenos pedaços sobre uma tela de aço, processado, centrifugado e lavado com PBS e meio de cultura, resultando em pellets celulares prontos para cultivo.
Como aumentar a chance de sucesso das culturas primárias?Uma das principais vantagens de uma cultura primária é a semelhança fenotípica das células cultivadas com sua contraparte no organismo. Contudo, para manter essa semelhança é necessário:
- Prover condições que permitam uma melhor adesão celular, como fornecimento de matriz extracelular apropriada ou condições para que as células possam produzir essa matriz. A maioria das células normais de um organismo precisam aderir para sobreviver e, em cultura, isso depende da secreção de moléculas de matriz extracelular que aderem ao fundo do frasco de cultura.
- Caso haja fornecimento de matriz extracelular, ajustar o tipo de matriz conforme o tipo de célula. A composição da matriz extracelular deve ser adequada para cada tipo celular, visto que ela influencia na adesão, sobrevivência e fenótipo das células.
- Ajustar a confluência celular inicial (durante o plaqueamento) e final conforme o tipo de célula, visto que isso influencia na sobrevivência, proliferação e expressão de funções características do tecido de origem.
- Fornecer fatores e moléculas sinalizadoras adequados para o tipo celular de interesse.
- Observar atentamente e continuamente as células cultivadas ao microscópio para conhecê-las e saber identificar fatores que podem estar levando a deterioração da cultura, como confluência inadequada, gradientes ou zonas com diferença de temperatura na incubadora, contaminação etc.
Para saber sobre esse tema assista a nossa videoaula e acesse o texto da transcrição:






