Módulo 8Ensaios de avaliação da viabilidade e proliferação celular
MÓDULO 8 – AULA 1
Ensaios de avaliação da viabilidade e proliferação celular
O que entendemos por “proliferação celular”?
Quando falamos em proliferação celular nos referimos ao aumento em número de uma determinada população de células. Através da divisão celular cada uma pode dar origem a células geneticamente iguais, mantendo as características do tipo celular.
Dependendo do tipo celular, a proliferação pode ser infinita, como no caso de células imortalizadas; ou pode ser limitada, como no caso das células primárias, que são células isoladas de diferentes tecidos. Na maior parte das vezes, células primárias precisam da adição de fatores de crescimento ou mitógenos para que a proliferação celular aconteça.
A proliferação é dirigida pelo ciclo celular, onde o DNA cromosomal da célula é duplicado (fase S, pela síntese de DNA) e segregado às duas células-filhas geradas (fase M, por mitose). As fases do ciclo celular são importantes, pois muitos fármacos são capazes de interferir no ciclo, levando à interrupção da proliferação e muitas vezes induzindo a morte celular. Devido ao aumento no material nuclear durante a fase S do ciclo, a proliferação pode ser monitorada pela adição de nucleotídeos marcados com fluorescência ou radioativamente.
O que significa o termo “viabilidade celular”?
Já a viabilidade celular faz referência à “vida da célula”, ou seja, à sua capacidade para manter as suas funções celulares, como metabolismo, divisão e forma. A manutenção de uma viabilidade celular ótima é imprescindível para a realização de ensaios envolvendo cultura de células, e também pode ser utilizada como parâmetro para avaliar a toxicidade de determinados compostos.
Diversos fatores podem atuar sobre as células, afetando a sua viabilidade: fatores físicos, químicos e biológicos. O sinal mais evidente da perda de viabilidade celular é a perda da integridade da membrana celular, que leva à perda de conteúdo intracelular. Na próxima seção serão abordados em detalhe estes fatores.
Na figura “Viabilidade x Proliferação” apresenta-se um resumo das informações descritas acima.
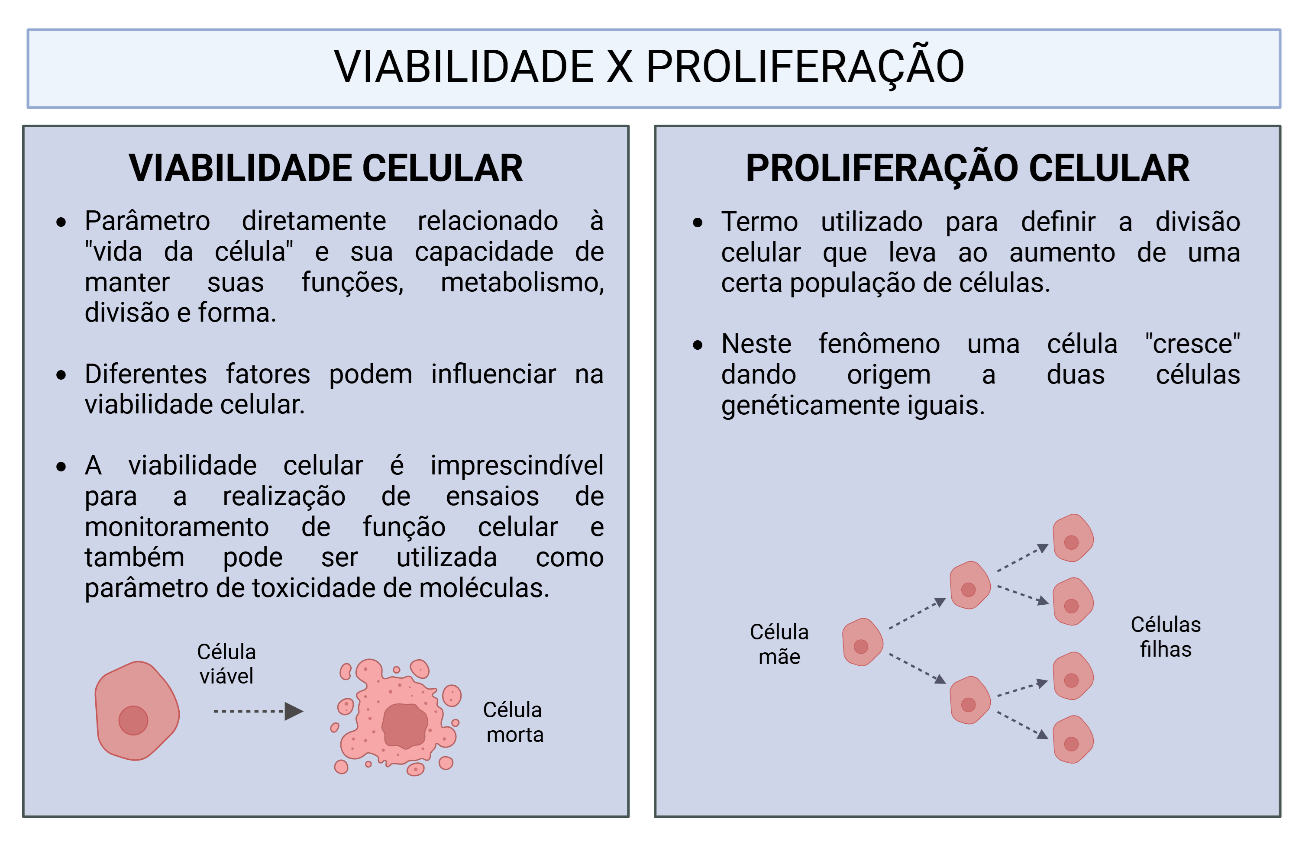 Viabilidade x Proliferação. Quadro comparativo apresentando os conceitos básicos relacionados a estes dois importantes parâmetros. Adaptado a partir de conteúdo de Alberts (2014) Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025). https://BioRender.com/k73n736 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: A imagem apresenta um quadro comparativo entre viabilidade celular e proliferação celular. No lado esquerdo, a viabilidade celular é definida como um parâmetro relacionado à capacidade de uma célula manter suas funções, metabolismo, divisão e forma. Vários fatores podem influenciar essa viabilidade, sendo um critério fundamental para monitoramento da função celular e avaliação da toxicidade de substâncias. A ilustração mostra uma célula viável representada como uma estrutura intacta e uma célula morta com membrana rompida e fragmentos ao redor. No lado direito, o conceito de proliferação celular é abordado. Esse termo refere-se à divisão celular, resultando no aumento da população de células. O fenômeno ocorre quando uma célula mãe se divide, originando duas células filhas geneticamente idênticas. A ilustração demonstra esse processo em um diagrama de progressão, onde uma célula inicial se divide sucessivamente, formando um grupo de células idênticas. A imagem destaca a importância de distinguir viabilidade celular, que mede a sobrevivência da célula, de proliferação celular, que indica o crescimento populacional por divisão celular.
Viabilidade x Proliferação. Quadro comparativo apresentando os conceitos básicos relacionados a estes dois importantes parâmetros. Adaptado a partir de conteúdo de Alberts (2014) Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025). https://BioRender.com/k73n736 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: A imagem apresenta um quadro comparativo entre viabilidade celular e proliferação celular. No lado esquerdo, a viabilidade celular é definida como um parâmetro relacionado à capacidade de uma célula manter suas funções, metabolismo, divisão e forma. Vários fatores podem influenciar essa viabilidade, sendo um critério fundamental para monitoramento da função celular e avaliação da toxicidade de substâncias. A ilustração mostra uma célula viável representada como uma estrutura intacta e uma célula morta com membrana rompida e fragmentos ao redor. No lado direito, o conceito de proliferação celular é abordado. Esse termo refere-se à divisão celular, resultando no aumento da população de células. O fenômeno ocorre quando uma célula mãe se divide, originando duas células filhas geneticamente idênticas. A ilustração demonstra esse processo em um diagrama de progressão, onde uma célula inicial se divide sucessivamente, formando um grupo de células idênticas. A imagem destaca a importância de distinguir viabilidade celular, que mede a sobrevivência da célula, de proliferação celular, que indica o crescimento populacional por divisão celular.
Quais fatores podem afetar a viabilidade celular?
- Osmolaridade: a concentração de solutos no meio de cultivo e soluções deve ser adequada pois pode interferir com o equilíbrio osmótico, alterando o volume celular consequentemente, afetando a viabilidade. Por exemplo, um meio com baixa osmolaridade induz a entrada de água na célula e aumento do seu volume, podendo levar à lise celular.
- Radiação: altos níveis de radiação como a ultravioleta podem ser perigosos para as células, onde mutações no DNA podem ser induzidas, levando a transformações ou alterações na sua viabilidade.
- Privação de nutrientes: baixas concentrações de substratos utilizados pelas células para o seu metabolismo energético e suas principais funções pode alterar a sua viabilidade, levando em muitos casos à morte celular.
- Contaminantes químicos e metabólitos: diversas moléculas podem afetar à viabilidade das células em cultivo, através de danos ao DNA ou afetando diferentes funções celulares, como o seu metabolismo.
- Falta de ancoramento: quando células aderentes, ou seja, que crescem unicamente aderidas a um substrato ou superfície, perdem a capacidade de adesão também podem ter a sua viabilidade afetada.
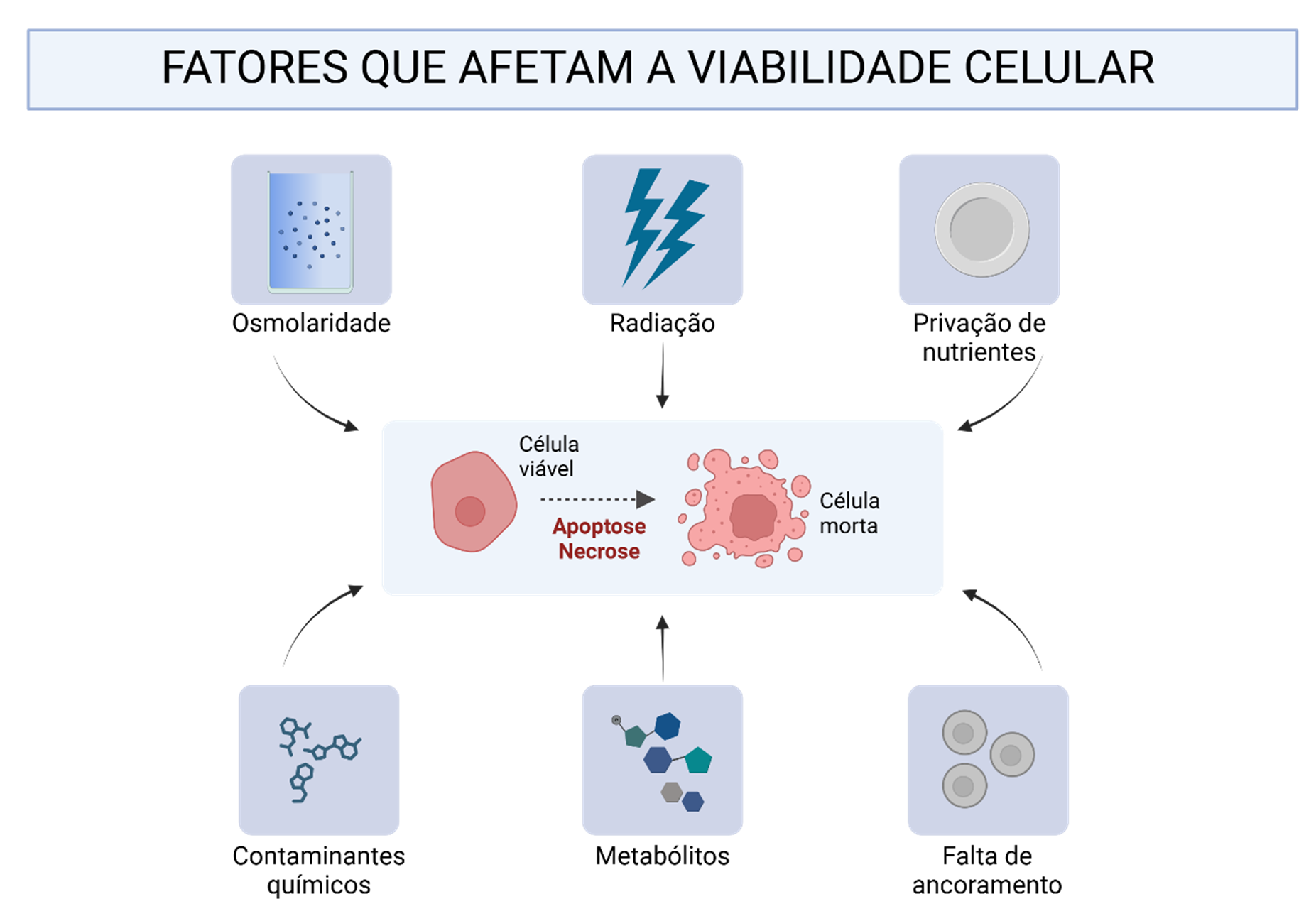
Fatores que afetam a viabilidade celular. A viabilidade das células em cultivo pode ser influenciada por diversos fatores físicos como radiação, temperatura, pressão até fatores químicos como contaminantes, osmolaridade e metabólitos ou mesmo condições inerentes aos cultivos celulares como privação de nutrientes ou presença ou ausência de metabólitos, entre outros. Adaptado a partir de conteúdo de Freshney (2010) e Alberts (2014) Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025). https://BioRender.com/r26r572 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: A imagem apresenta um esquema central com uma célula viável e seu processo de morte celular, seja por apoptose ou necrose. Ao redor desse esquema, há seis ícones representando diferentes fatores que afetam a viabilidade celular. 1) Presença de contaminantes – Representado por uma solução contendo partículas, simbolizando agentes externos que podem comprometer a viabilidade celular. 2) Radiação ou estresse físico – Ilustrado por um ícone de raios, simbolizando radiação ou choque térmico. 3) Fatores de cultura – Mostrado como uma placa de cultura, representando a influência do ambiente de cultivo na viabilidade celular. 4) Presença de substâncias químicas ou fármacos – Representado por estruturas químicas, indicando a influência de substâncias tóxicas ou drogas. 5) Osmolaridade e metabólitos – Ilustrado por moléculas, destacando o impacto da concentração iônica e metabólitos celulares. 6) Privação de nutrientes – Representado por um conjunto de células, simbolizando o efeito da falta de nutrientes no meio de cultura. A imagem reforça que diversos fatores podem induzir a morte celular, sendo essencial monitorá-los para garantir a manutenção de células viáveis em cultivo.
Como pode ser avaliada a proliferação celular?
Existem diversos métodos que utilizam diferentes parâmetros celulares para quantificar a proliferação celular. Na figura abaixo (“Parâmetros para análise da proliferação celular”) são apresentadas algumas metodologias que permitem medir a proliferação celular.
A contagem de células, seja manualmente por câmara de Neubauer ou de forma automatizada através da citometria de fluxo, é uma das técnicas mais utilizadas para monitorar o crescimento celular. O aumento do número de células muitas vezes também é utilizada como técnica para avaliação da proliferação celular, que muitas vezes deve ser também confirmada por outras metodologias. Por que razão? Como mencionado anteriormente, a proliferação celular está associada ao aumento na quantidade de células e, portanto, de material genético, e o padrão ouro na avaliação da proliferação celular é justamente o uso de metodologias que avaliam o aumento do conteúdo do DNA. A duplicação do DNA pode ser avaliada a través de diferentes técnicas, como a incorporação de precursores de nucleotídeos (Ex: BrdU) ou pela quantificação do conteúdo por corante com afinidade, como DAPI ou iodeto de propídeo (PI) em técnicas que avaliam por exemplo as fases do ciclo celular. Com a proliferação celular, proteínas próprias do ciclo celular como Ki67 serão expressas e podem ser utilizadas como marcadores do ciclo celular, permitindo monitorar o aumento na população.
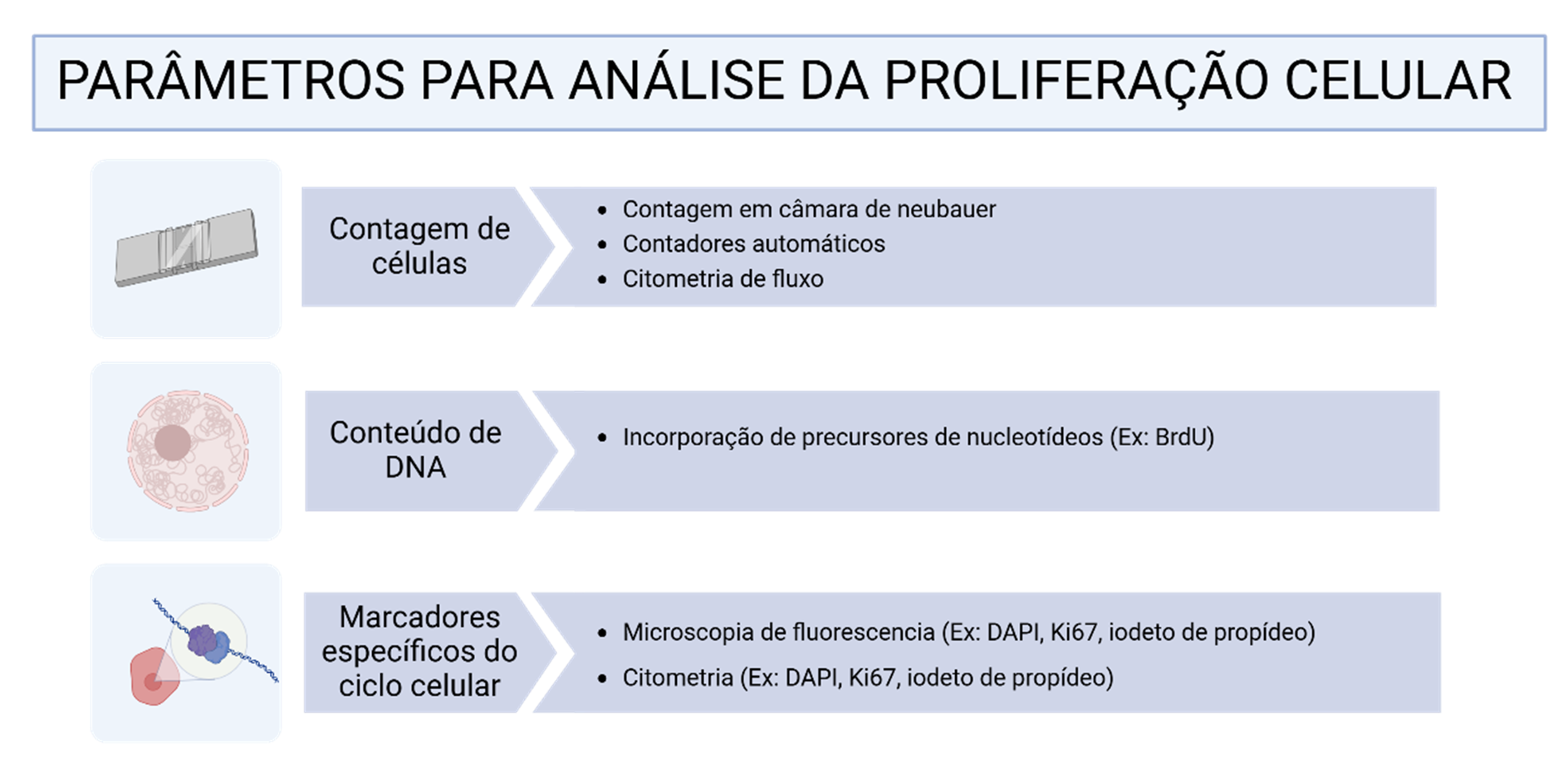
Parâmetros para análise da proliferação celular. A proliferação celular é associada ao aumento do número de células e muitas vezes pode ser determinada por metodologias de contagem, contudo muitas vezes é necessária a confirmação da proliferação celular por metodologias que avaliam o conteúdo de DNA durante a divisão celular, como a incorporação de precursores de nucleotídeos ou marcadores associados ao ciclo celular, sejam marcadores como o Ki67 que é expresso apenas em células em processo de divisão celular ou avaliação de fases do ciclo celular pela avaliação do conteúdo do DNA. Adaptado a partir de conteúdo de Freshney (2010) e Alberts (2014) Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025). https://BioRender.com/b41s697 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: A imagem apresenta três abordagens principais para análise da proliferação celular, organizadas em uma estrutura de fluxograma: 1) Contagem de células – Métodos utilizados para quantificar células, incluindo: Contagem manual em câmara de Neubauer. Uso de contadores automáticos para maior precisão. Citometria de fluxo, que permite uma análise em larga escala da população celular. 2) Conteúdo de DNA – Avaliação da síntese de DNA e proliferação celular por: Incorporação de precursores de nucleotídeos, como BrdU (Bromodeoxiuridina), que se incorpora ao DNA em replicação, possibilitando a detecção de células em divisão. 3) Marcadores específicos do ciclo celular – Métodos de detecção da atividade celular proliferativa por: Microscopia de fluorescência usando DAPI, Ki67 ou iodeto de propídio. Citometria de fluxo, permitindo quantificar células em diferentes fases do ciclo celular com base no conteúdo de DNA. A figura destaca múltiplas estratégias complementares para monitoramento da proliferação celular, sendo aplicáveis conforme a necessidade do experimento.
E se quisermos avaliar viabilidade, quais métodos podemos utilizar?
O monitoramento da viabilidade celular durante a manutenção das culturas celulares e prévio à realização dos diferentes experimentos é essencial para garantir que as células utilizadas serão capazes de responder aos estímulos e condições experimentais adequadamente. Na figura abaixo (“Parâmetros para análise da viabilidade celular”) são descritos alguns métodos que permitem avaliar a viabilidade celular.
Uma das metodologias mais amplamente utilizadas para medir viabilidade é a verificação da integridade da membrana plasmática, pois uma vez que a integridade da membrana foi perdida, a célula não é mais capaz de desempenhar suas funções. A perda de integridade da membrana leva ao aumento de sua permeabilidade e permite a utilização de corantes vitais que marcam o conteúdo intracelular de células não viáveis, enquanto as células viáveis não são coradas, permitindo a sua identificação e contagem. O método da exclusão de Azul de Tripan é baseado na integridade da membrana celular, sendo um dos mais utilizados para determinação da viabilidade celular.
O comprometimento na viabilidade celular pode levar a diferentes tipos de morte celular, como apoptose e necrose. Na apoptose, o fosfolipídeo fosfatidilserina (PS) é exposto à monocamada externa da membrana plasmática, sinalizando este tipo de morte celular. Assim, a PS pode ser utilizada como marcador de membrana para identificar células em processo de apoptose. A anexina é uma molécula com afinidade por PS e é comumente utilizada em experimentos de citometria para identificar morte celular. A fim de distinguir apoptose de necrose, onde a integridade da membrana plasmática é perdida, o corante PI é empregado junto à anexina nesse tipo de experimentos.

Parâmetros para análise da viabilidade celular. A viabilidade celular por técnicas simples como a contagem celular em câmara de Neubaer com uso do corante vital Azul de Tripan, normalmente realizada rotineiramente na manutenção de cultivo celular, ou uso de outros métodos como durante experimentos, seja a contagem direta por citometria de fluxo, em equipamentos ou com uso de kits para essa finalidade ou ensaios de marcadores de membrana como o ensaio da anexina / PI. Ensaios colorimétricos também podem ser utilizados para avaliação da viabilidade celular relativa a um controle. Adaptado a partir de conteúdo de Freshney (2010) e Alberts (2014) Fonte: Criado em BioRender. Melo de Aguiar, A., Barisón, M.J. (2025). https://BioRender.com/c57h942 Sob licença CC-BY 4.0 (https://creativecommons.org/licenses/by/4.0/). Descrição estendida da legenda: A figura apresenta três abordagens principais para análise da viabilidade celular, organizadas em um fluxograma: 1) Integridade da membrana plasmática – Avaliação da viabilidade celular pela incorporação de corantes vitais, como: Azul de Tripan – Utilizado na contagem celular manual para distinguir células viáveis (transparentes) de células mortas (coradas). Iodeto de Propídio (PI) – Corante fluorescente que penetra apenas em células com membranas comprometidas, sendo analisado por microscopia de fluorescência ou citometria de fluxo. 2) Marcadores de membrana – Métodos específicos para detecção de morte celular: Anexina V – Liga-se à fosfatidilserina, um marcador precoce de apoptose. PI e Anexina V – A combinação desses dois corantes permite diferenciar células viáveis, apoptóticas e necróticas por citometria de fluxo. 3) Ensaios colorimétricos em microplacas – Avaliação quantitativa da viabilidade celular baseada na atividade metabólica: MTT – Corante metabólico usado para medir a viabilidade de células aderentes e não aderentes. Vermelho Neutro – Método para quantificar células aderentes vivas, baseado na capacidade de retenção do corante em lisossomos ativos. Ambos os ensaios são frequentemente utilizados para avaliar a toxicidade de compostos ou a proliferação celular. A figura destaca diferentes estratégias para monitoramento da viabilidade celular, cada uma adequada a uma necessidade experimental específica.
Para saber mais sobre esse tema, assista a nossa videoaula e acesse o texto da transcrição:
Saiba mais em conteúdos do curso: No módulo de técnicas básicas e de equipamentos é possível saber mais contagem celular em câmara de Neubaer e avaliação da viabilidade celular por Azul de Tripan.
Vamos testar seus conhecimentos no tema desse módulo?
Confira uma pergunta por vez
O ensaio de incorporação de precursores de nucleotídeos é comumente utilizado para medir:
-
A) Viabilidade celular
-
B) Proliferação celular
Ki67, uma proteína específica do ciclo celular é utilizada como marcadora para verificar viabilidade celular.
-
A) Verdadeiro
-
B) Falso






